Można temu zaradzić w różny sposób - tutaj opiszę metodą "lania kwasu"
Dla większości akwariów jest to najtańsza metoda poprawy jakości wody do celów akwarystyki roślinnej. Twardość węglanowa ma większy wpływ na rośliny i glony, niż twardość ogólna. Ta ostatnia może być całkiem wysoka i nic złego się nie dzieje. To twardość węglanowa odpowiada za większość problemów.
Z odczynem zasadowym wody mamy do czynienia w obecności jonów wodorotlenowych OH. Mogą one pochodzić z "klasycznych" zasad - wodorotlenków, np. NaOH. Oczywiście w akwarium nie mamy zwykle z nimi do czynienia, chyba, że ktoś czyścił studnię za pomocą wapna gaszonego (na wsiach takie praktyki się zdarzają). Zachodzi wtedy reakcja CaO + H2O --> Ca(OH)2. Część wodorotlenku wapnia ulega reakcjom sprzyjającym oczyszczeniu wody, ale część pozostaje w wodzie zwiększając odczyn wody (pH). Kiedyś rozmawiałem z rolnikiem i mówił, że taka woda "pali bebechy, i widać, że jest dobra"
Znacznie częściej z odczynem zasadowym mamy do czynienia w obecności soli mocnych zasad z słabymi kwasami. Są to kwasy: octowy, cytrynowy, fosforowy i najpowszechniejszy węglowy. Wskutek reakcji tych soli z wodą zachodzi proces hydrolizy w wyniku którego odtwarzany jest kwas, który pozostaje w postaci niezdysocjowanej i powstaje zdysocjowana zasada nadająca odczyn zasadowy wodzie, przykładowo: NaHCO3 + H2O --> H2CO3 + NaOH, ten ostatni jest w postaci zdysocjowanej a więc tworzy jony Na i OH (odpowiednio z plusem i minusem). Stąd, aby doprowadzić pH do odczynu obojętnego należy zobojętnić powstającą zasadę za pomocą mocnego kwasu (solny, siarkowy, azotowy). Zachodzi wtedy klasyczna reakcja zobojętniania, np. HCl + NaOH --> NaCl + H2O a powstająca sól (NaCl), która jest całkowicie zdysocjowana nie zmienia pH wody.
W akwarium mamy najczęściej do czynienia z obecnością węglanów i wodorowęglanów wapnia, magnezu i sodu. Podwyższają one pH wody właśnie wskutek hydrolizy tych soli. Aby doprowadzić wodę do obojętnego pH należy zużyć odpowiednią ilość kwasu. To, ile należy zużyć kwasu określa parametr zwany "zasadowością" roztworu. I jest to parametr wyznaczany w testach na twardość węglanową. Wartość parametru można podać w różnych jednostkach, m.in. w stopniach niemieckich co się często praktykuje. To, że powoduje to sporo nieporozumień już opisywałem.
A teraz jak w praktyce stwierdzić ile należy dodać jakiego kwasu aby osiągnąć spadek pH, i kH do zadanej wartości. Otóż nie jest to tak oczywiste jak w przypadku np. mieszania wody RO z wodą twardą, gdzie w banalny sposób można wyznaczyć twardość wody po zmieszaniu. Wynika to z tego, że pH jest parametrem, który określa 10-cio krotne zmiany stężenia jonów H (i równocześnie OH). Stąd dodawanie jednakowych ilości pewnej cieczy o pewnym pH do innej cieczy o drugim pH nie uzyskuje się pH wyznaczanego w prosty sposób jako połowa wartości leżącej pomiędzy poprzednimi wartościami pH.
Zobaczcie wykres zobojętniania zasady za pomocą kwasu:

Jak widać, czysta woda natychmiast po dodatku już małej ilości kwasu osiąga szybko małą wartość pH. Gdy w wodzie znajduje się układ buforowy (np. wspomniane węglany) to najpierw zachodzi zobojętnianie tych węglanów z lekkim spadkiem pH a dopiero później gwałtowny spadek.
Zakwaszając wodę "kranówkę" kwasem obserwuje się z reguły bardzo powolny spadek pH mimo lania relatywnie dużych ilości kwasu a po przekroczeniu pewnego punktu dodanie 1 kropli kwasu powoduje spadek pH o kilka jednostek.
Stąd zakwaszanie wody w akwarium musi przebiegać bardzo ostrożnie. Formalnie można policzyć ilość kwasu potrzebną do zobojętnienia układu buforowego w akwarium. Na to pozwala przykładowo mój kalkulator.
Jeszcze jeden problem... Jak powiązać spadek kH z pH wody, tj. o ile trzeba zmienić kH, aby pH zmieniło się "ileś tam"? Zobaczcie na tabelę zawartości CO2 od kH i pH:
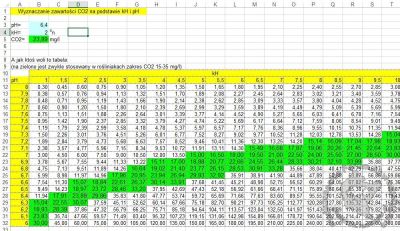
Bez dozowania sztucznego CO2 jego zawartość leży w granicach 4 ppm (zaznaczone na czerwono w tabeli). Znając pH lub kH znamy drugi z parametrów. Jeżeli chcemy zmienić pH z 8 na 7 to prawdopodobnie mamy twardość kH rzędu 10. Obliczenia w moim kalkulatorze należałoby więc tak prowadzić, aby uzyskać zmianę kH o 9 jednostek (zejście z kH od 10 do 1 co odpowiada pH od 8 do 7).
Wszelkie "wypadki przy pracy" mogą spowodować gwałtowny spadek pH i zabicie całej obsady w akwarium. Stąd zakwaszanie należy dokonywać wyłącznie na wodzie do podmian i to tak, aby pH nie spadło zbyt drastycznie poniżej oczekiwanej wartości. Wtedy łącząc z wodą w akwarium można oczekiwać, że przy kilku podmianach dojdziemy do właściwego poziomu pH i kH w zbiorniku. Pamiętajmy też, że ryby i rośliny nie lubią drastycznych zmian pH wody nawet w tolerowanym zakresie. Przyjmuje się, e dobowa zmiana pH nie powinna być większa niż 0,2.
Tu jesy "sprawdzony" schemat dotyczący zakwaszania wody w akwarium z netu: http://akwarystyka.com.pl/showpost.php? ... stcount=14
Dla mnie opis jest jednak minimalnie zagmatwany i metoda mieszania dosyć niepraktyczna więc sam osobiście polecałbym robić to tak:
- poprosić jakiegoś chemika o zrobienie kwasu małym stężeniu (kwas jest bardzo niebezpieczny więc dla własnego zdrowia zostawmy to chemikom), np. 1-5% - taki kwas jest już na tyle bezpieczny dla zdrowia ile środki do czyszczenia kibli itp.
- w kalkulatorze wyznaczymy ile nam trzeba kwasu do podmienianej wody. Załóżmy, że podmieniamy 100 l wody o kH = 10 i chcemy zbić do 7 (spadek kH około 3). Pierwsze to wpis do kalkulatora ilości wody (100 l). Schodząc na dół kalkulatora odnajdujemy kwas, który mamy (np. siarkowy) i wpisujemy jego stężenie, np. 10% i kombinujemy objętość dodawanego kwasu tak, aby wyszła nam zadana wartość spadku kH (tutaj około 3).
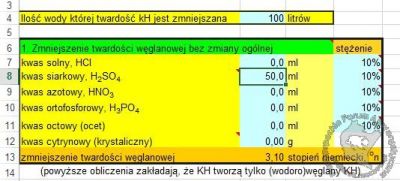
- Pierwszy raz musimy zrobić testy a więc bierzemy troszeczkę (a nawet połowę) mniej tego co chcielibyśmy osiągnąć. To co wpisaliśmy wydaje się być dobre (chcieliśmy zmniejszyć o 10 ppm a według obliczeń jest to 7,72 - więc może być). Teoretycznie więc jeżeli dodamy ten kwas do podmienianej wody to będziemy mieć kH rzędu 2-3. Jakiś zapas bezpieczeństwa więc jest. A więc wlewamy ten 1 ml kwasu 1% do tych 10 l wody do podmiany. Po dokładnym wymieszaniu musimy odczekać kilka godzin, najlepiej dobę. Po tym czasie mierzymy pH. Jeżeli jest dobrze to siup do akwarium. Jeżeli jest za niskie (np. poniżej 6,5) to do wiadra dolewamy trochę wody z kranu. Jeżeli pH jest za wysokie dodajemy jeszcze troszkę kwasu. Odczekujemy i mierzymy ponownie. Jak wszystko już wiemy o tym "jak nasza" kranówka reaguje na dodatek kwasu to kolejny raz znamy ilość kwasu i ilość wody, więc mieszamy to, odczekujemy dobę i mierzymy pH.
Ten pomiar pH nie jest obowiązkowy, ale rekomendowany ponieważ woda w kranie czasem zmienia skład. Jeżeli podmiana nie jest duża a różnica w kH duża (na początku naszej zabawy ze zmianą kH) to nawet jak lekko przesadzimy z kwasem (ale lekko) to woda w akwarium nie ulegnie znaczącemu zakwaszeniu bo ma przecież sporo buforu. Późniejsze zakwaszanie wody do podmian, gdy w akwa mamy już np. kH = 4 należy wykonywać jednak bardzo precyzyjnie z obowiązkowym testem pH.
============== Ciekawostki i nowinki =================
Zamiast stosować niebezpieczne, czasem trudne do kupienia kwasy mineralne możemy zastosować biodegradowalny kwasek cytrynowy. Obliczeń w kalkulatorze nie ma więc aby ustalić ilość kwasku musicie sypać go do wiaderka i mierzyć pH podobnie jak wyżej. Kwas cytrynowy jest kwasem biodegradowalnym a więc bakterie przerabiają go na substancje prostsze, m.in. CO2. Jest więc dodatkowym źródłem CO2 w akwarium. Ostatnie informacje jakie znalazłem to takie, że kwas cytrynowy i jego sole znajdują zastosowanie w preparatach typu "węgiel w płynie". Okazuje się więc, że taki preparat moglibyśmy nawet produkować sami w domu z kwasku cytrynowego i sody oczyszczonej. Jeżeli ktoś ma reaktor chemiczny do wytwarzania CO2 to miałby gotowy cytrynian sodu w dowolnych ilościach.